Характеристики ковалентной связи. Ковалентная связь. Метод валентных связей
Содержание.
I.Химическая связь. 2
II.Ковалентная связь.
1.Методы изучения ковалентной связи. 2
B.Метод валентных связей. 3
C.Метод молекулярных орбиталей. 5
1.Свойства ковалентной связи. 7
2.1. Длина связи. 7
2.2. Энергия связи. 9
2.3. Кратность ковалентной связи. 11
2.4. Насыщаемость ковалентной связи. 13
2.5. Направленность ковалентной связи. 14
2.6. Полярность и поляризуемость ковалентной связи. 16
2.7. Гибридизация. 18
3. Донорно-акцепторный механизм образования ковалентной связи. 20
III. Литература. 23
Химическая связь.
Химическую связь можно определить как взаимодействие двух или нескольких атомов, в результате которого образуется химически устойчивая многоатомная микросистема (молекула, кристалл, комплекс и др.).
Учение о связи занимает центральное место в современной химии, поскольку химия как таковая начинается там, где кончается изолированный атом и начинается молекула. В сущности, все свойства веществ обусловлены особенностями связей в них. Главное отличие химической связи от других видов взаимодействия между атомами заключается в том, что ее образование определяется изменением состояния электронов в молекуле по сравнению с исходными атомами. Теория связи должна дать ответы на ряд вопросов. Почему образуются молекулы? Почему одни атомы вступают во взаимодействие, а другие – нет? Почему атомы соединяются в определенных соотношениях? Почему атомы располагаются в пространстве определенным образом? И наконец, надо рассчитать энергию связи, ее длину и другие количественные характеристики.
В большинстве случаев при образовании связи происходит обобществление электронов связываемых атомов. Такой тип химической связи называют ковалентной связью (приставка "ко-" в латинском языке означает совместность, "валенс" - имеющий силу). Связывающие электроны находятся преимущественно в пространстве между связываемыми атомами. За счет притяжения ядер атомов к этим электронам образуется химическая связь. Таким образом, ковалентная связь - это химическая связь, возникающая за счет увеличения электронной плотности в области между химически связанными атомами.
Ковалентная связь.
Методы изучения ковалентной связи.
В настоящее время для изучения химической связи в основном используют два метода: 1) валентных связей; 2) молекулярных орбиталей. 1.1. Метод валентных связей.
В рамках первого метода рассматривают индивидуальные атомы, вступающие во взаимодействие, исходя из принципа завершенности электронной оболочки (правило октета). Ковалентная связь с точки зрения метода валентных связей образуется за счет обобществления электронной пары.
Рассмотрим квантово-механическую модель ковалентной связи по методу валентных связей на примере молекулы водорода.
В 1927 г. уравнение Шрёдингера было решено для молекулы водорода немецкими физиками В.Гейтлером и Ф.Лондоном. Это была первая удачная попытка применения квантовой механики к решению проблем связи. Их работа заложила основы метода валентных связей, или валентных схем.

Рис.1 Фото. Ф. Лондон. Рис.2. Фото. В.Гейтлер.
Результаты расчета можно представить графически в виде зависимостей сил взаимодействия между атомами (рис.3, а) и энергии системы (рис. 3, б) от расстояния между ядрами атомов водорода. Ядро одного из атомов водорода поместим в начало координат, а ядро второго будем приближать к ядру первого атома водорода вдоль оси абсцисс. Если спины электронов антипараллельны, силы притяжения (рис. 3, а, кривая I) и силы отталкивания (кривая II) будут нарастать. Результирующая этих сил представлена кривой III. Сначала преобладают силы притяжения, затем – отталкивания. Когда расстояние между ядрами становится равным r 0 = 0,074 нм, сила притяжения уравновешивается силой отталкивания. Равновесию сил соответствует минимальная энергия системы (рис. 3, б, кривая IV) и, следовательно, наиболее устойчивое состояние. Глубина «потенциальной ямы» представляет энергию связи Е 0 Н–Н в молекуле Н 2 при абсолютном нуле. Она составляет 458 кДж/моль. Однако при реальных температурах на разрыв связи требуется несколько меньшая энергия Е Н–Н , которая при 298К (25 °С) равна 435 кДж/моль. Разность этих энергий в молекуле Н 2 является энергией колебаний атомов водорода (Е кол = Е 0 Н–Н – Е Н–Н = 458 – 435 = 23 кДж/моль).
 Рис. 3. Зависимость сил взаимодействия атомов (а) и энергии системы (б)
Рис. 3. Зависимость сил взаимодействия атомов (а) и энергии системы (б)
от расстояния между ядрами атомов в молекуле Н
2
При сближении двух атомов водорода, содержащих электроны с параллельными спинами, энергия системы постоянно увеличивается (рис. 3, б, кривая V) и связь не образуется.
Таким образом, квантово-механический расчет дал количественное объяснение связи. При наличии у пары электронов противоположных спинов электроны двигаются в поле обоих ядер. Между ядрами появляется область с высокой плотностью электронного облака – избыточного отрицательного заряда, который стягивает положительно заряженные ядра. Из квантово-механического расчета следуют положения, являющиеся основой метода валентных связей:
Причиной связи является электростатическое взаимодействие ядер и электронов.
2. Связь образуется электронной парой с антипараллельными спинами.
3. Насыщаемость связи обусловлена образованием электронных пар.
4. Прочность связи пропорциональна степени перекрывания электронных облаков.
5. Направленность связи обусловлена перекрыванием электронных облаков в области максимальной электронной плотности.
Простой метод валентных связей для химика наиболее понятен, удобен и нагляден, лучше всего отвечает целям первичного обучения. Недостаток метода валентных связей состоит в том, что в его рамках нельзя объяснить некоторые экспериментальные данные.
Метод молекулярных орибиталей.
Большей эффективностью обладает метод молекулярных орбиталей, в котором рассматриваются электроны, находящиеся в поле притяжения, созданном всеми атомными ядрами молекулы. С точки зрения метода молекулярных орбиталей в молекуле нет атомов как таковых, а есть взаимно отталкивающиеся ядра и взаимодействующие с ними и между собой электроны.
Метод молекулярных орбиталей (МО) наиболее нагляден в его графической модели линейной комбинации атомных орбиталей (ЛКАО). Метод МО ЛКАО основан на следующих правилах.
1. При сближении атомов до расстояний химических связей из атомных орбиталей образуются молекулярные.
2. Число полученных молекулярных орбиталей равно числу исходных атомных.
3. Перекрываются атомные орбитали, близкие по энергии. В результате перекрывания двух атомных орбиталей образуются две молекулярные. Одна из них имеет меньшую энергию по сравнению с исходными атомными и называется связывающей , а вторая молекулярная орбиталь обладает большей энергией, чем исходные атомные орбитали, и называется разрыхляющей .
4. При перекрывании атомных орбиталей возможно образование и -связи (перекрывание по оси химической связи), и -связи (перекрывание по обе стороны от оси химической связи).
5. Молекулярная орбиталь, не участвующая в образовании химической связи, носит название несвязывающей . Ее энергия равна энергии исходной АО.
6. На одной молекулярной орбитали (как, впрочем, и атомной) возможно нахождение не более двух электронов.
7. Электроны занимают молекулярную орбиталь с наименьшей энергией (принцип наименьшей энергии).
8. Заполнение вырожденных (с одинаковой энергией) орбиталей происходит последовательно по одному электрону на каждую из них.
Применим метод МО ЛКАО и разберем строение молекулы водорода. Изобразим на двух параллельных диаграммах энергетические уровни атомных орбиталей исходных атомов водорода
Рис. 4 Энергетическая диаграмма несвязанных атомов водорода.Далее мысленно перекроем две атомные орбитали, образовав две молекулярные, одна из которых (связывающая) обладает меньшей энергией (расположена ниже), а вторая (разрыхляющая) – большей энергией (расположена выше) (рис. 5).
Рис. 5 Диаграмма уровней энергии АО атомов H и МО молекулы H 2Видно, что имеется выигрыш в энергии по сравнению с несвязанными атомами. Свою энергию понизили оба электрона, что соответствует единице валентности в методе валентных связей (связь образуется парой электронов).
Хотя метод молекулярных орбиталей
более строг и универсален
, он позволяет полнее объяснить экспериментальные данные.
III.Свойства ковалентной связи.
Свойства ковалентной связи: энергия, длина, полярность, насыщаемость, направленность, гибридизация, кратность.
2.1.Длина химической связи.
При образовании химической связи всегда происходит сближение атомов - расстояние между ними меньше, чем сумма радиусов изолированных атомов:
r (A−B) < r (A) + r (B). Радиус атома водорода составляет 0,053 нм, атома фтора – 0,071 нм, а расстояние между ядрами атомов в молекуле HF равно 0,092 нм:

Межъядерное расстояние между химически связанными атомами называется длиной химической связи.
Во многих случаях длину связи между атомами в молекуле вещества можно предсказать, зная расстояния между этими атомами в других химических веществах. Длина связи между атомами углерода в алмазе равна 0,154 нм, между атомами галогена в молекуле хлора – 0,199 нм. Полусумма расстояний между атомами углерода и хлора, рассчитанная из этих данных, составляет 0,177 нм, что совпадает с экспериментально измеренной длиной связи в молекуле CCl 4 . В то же время это выполняется не всегда. Например, расстояние между атомами водорода и брома в двухатомных молекулах составляет 0,074 и 0,228 нм, соответственно. Среднее арифметическое этих чисел составляет 151 нм, однако реальное расстояние между атомами в молекуле бромоводорода равно 141 нм, то есть заметно меньше.
Расстояние между атомами существенно уменьшается при образовании кратных связей. Чем выше кратность связи, тем короче межатомное расстояние .
Длины некоторых простых и кратных связей.
2.2. Энергия связи . Химическая связь возникает лишь в том случае, если полная энергия взаимодействующих атомов уменьшается, т.е. при образовании связи должна всегда выделяться энергия. Количество энергии, выделяющейся при образовании химической связи, называется энергией связи E СВ (кДж/моль).Энергия связи является мерой прочности связи. Чем больше выделяется энергии при образовании молекулы, тем больше энергии надо затратить на разрыв, т.е. тем молекула прочнее.
Химическое соединение образуется из отдельных атомов только в том случае, если это энергетически выгодно. Если силы притяжения преобладают над силами отталкивания, потенциальная энергия взаимодействующих атомов понижается, в противном случае − повышается. На некотором расстоянии (равном длине связи r 0 ) эта энергия минимальна.

Рис. 6. Энергия химической связи.
Таким образом, при образовании химической связи энергия выделяется, при ее разрыве − поглощается. Энергия E 0 , необходимая для того, чтобы разъединить атомы и удалить их друг от друга на расстояние, на котором они не взаимодействуют, называется энергией связи . Для двухатомных молекул энергия связи определяется как энергия диссоциации молекулы на атомы. Она может быть измерена экспериментально. В молекуле водорода энергия связи численно равна энергии, которая выделяется при образовании молекулы Н 2 из атомов Н: Н + Н = Н 2 + 432 кДж. Эту же энергию нужно затратить, чтобы разорвать связь Н-Н: H 2 = H + H − 432 кДж.
Для многоатомных молекул эта величина является условной и отвечает энергии такого процесса, при котором данная химическая связь исчезает, а все остальные остаются без изменения. При наличии нескольких одинаковых связей (например, для молекулы воды, содержащей две связи кислород−водород) их энергию можно рассчитать, используя закон Гесса . Величины энергии распада воды на простые вещества, а также энергии диссоциации водорода и кислорода на атомы известны: 2Н 2 О = 2Н 2 + О 2 ; 484 кДж/моль
Н 2 = 2Н; 432 кДж/моль
О 2 = 2О; 494 кДж/моль
Учитывая, что в двух молекулах воды содержится 4 связи, энергия связи кислород-водород равна:
Е (О−Н) = (2 . 432 + 494 + 484) / 4 = 460,5 кДж/моль
В молекулах состава AB n последовательный отрыв атомов В сопровождается определенными (не всегда одинаковыми) затратами энергии. Например, значения энергии (кДж/моль) последовательного отщепления атомов водорода от молекулы метана существенно различаются:
При этом энергия связи А−В определяется как средняя величина затраченной энергии на всех стадиях:СН 4 = С + 4Н; 1649 кДж/моль
Е (С−Н) = 1649 / 4 = 412 кДж/моль
Чем выше энергия химической связи, тем прочнее связь . Связь считается прочной, или сильной, если ее энергия превышает 500 кДж/моль (например, 942 кДж/моль для N 2 ), слабой - если ее энергия меньше 100 кДж/моль (например, 69 кДж/моль для NO 2 ). Если при взаимодействии атомов выделяется энергия менее 15 кДж/моль, то считают, что химическая связь не образуется, а наблюдается межмолекулярное взаимодействие (например, 2 кДж/моль для Xe 2 ). Прочность связи обычно уменьшается с увеличением ее длины.
Одинарная связь всегда слабее, чем кратные связи - двойная и тройная - между теми же атомами.Энергии некоторых простых и кратных связей.
Кратность ковалентной связи.
Кратность ковалентной связи или делоколизация связи - число связей, образующихся между атомами, называется кратностью (порядком) связи. С увеличением кратности (порядка) связи изменяется длина связи и ее энергия. Относительно линии соединяющей центры атомов образующих связь различают σ и π -связь (рис.9).

Рис. 7. Схема образования связей в молекуле азота: а) σ - связей; б) π – связей.
Связь, образованная перекрыванием электронных облаков по оси, проходящей через ядра атомов, называется σ -связью.
 Рис. 8. Примеры
σ
-связей
Рис. 8. Примеры
σ
-связей
Связь, образованная перекрыванием электронных облаков по обе стороны от оси, проходящей через ядра атомов, называется π -связью. Примеры π -связи приведены на рис. 9 . Такое перекрывание энергетически менее выгодно, чем по σ -типу. Оно осуществляется периферийными частями электронных облаков с меньшей электронной плотностью. Увеличение кратности связи означает образование π -связей, которые имеют меньшую энергию по сравнению с σ -связью. В этом и есть причина нелинейного увеличения энергии связи в сравнении с увеличением кратности.
 Рис. 9. Примеры
π
–связей
Рис. 9. Примеры
π
–связей
Насыщаемость ковалентной связи.
Атом не может образовать бесконечное число ковалентных связей, оно вполне определенное. Максимальное число связей, которое может образовать атом, определяется числом его валентных электронных орбиталей. Это и определяет насыщаемость ковалентной связи. Благодаря насыщаемости связей молекулы имеют определенный состав. Численное значение валентности в методе валентных связей определяется числом ковалентных связей, которые атом образует с другими атомами. Рассмотренный для молекулы Н 2 механизм образования связи парой электронов с антипараллельными спинами, принадлежавших до образования связи разным атомам, называется обменным. Если учитывать только обменный механизм, валентность атома определяется числом его неспаренных электронов.
Очевидно, что число ковалентных связей не может превышать числа образующих связи электронных пар. Однако насыщаемость как свойство ковалентной связи означает также, что если атом имеет некоторое количество неспаренных электронов, то все они должны участвовать в образовании ковалентных связей. Это свойство объясняется принципом наименьшей энергии. При образовании каждой дополнительной связи выделяется дополнительная энергия. Поэтому все валентные возможности реализуются полностью. Действительно, устойчива молекула Н 2 S, а не НS , где имеется нереализованная связь (неспаренный электрон обозначают точкой). Частицы, содержащие неспаренные электроны, называют свободными радикалами. Они чрезвычайно реакционноспособны и вступают в реакции с образованием соединений, содержащих насыщенные связи.
Направленность ковалентной связи.
Другое важное свойство ковалентной связи - ее направленность в пространстве. Направленность связи обусловливает пространственную структуру молекул, т. е. их геометрическую форму. Рассмотрим примеры.
В молекуле фтора F 2 связь образована 2р-орбиталями атомов фтора:
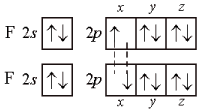
Наибольшая плотность электронного облака у 2р-орбитали в направлении оси симметрии. Если неспаренные электроны атомов фтора находятся на 2р х -орбиталях, связь осуществляется в направлении оси х (рис.10). На 2р y - и 2р z -орбиталях находятся неподеленные электронные пары, не участвующие в образовании связей (на рис. 10 заштрихованы).
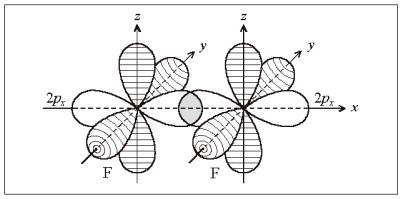 Рис. 10. Образование молекулы F
2
Рис. 10. Образование молекулы F
2
В молекуле фтороводорода НF связь образована 1s-орбиталью атома водорода и 2р х -орбиталью атома фтора:

Направленность связи в этой молекуле определяется ориентацией 2р х -орбитали атома фтора (рис. 11). Перекрывание происходит в направлении оси симметрии х. Любой другой вариант перекрывания энергетически менее выгоден.
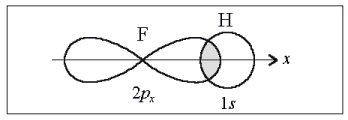 Рис. 11. Образование молекулы НF
Рис. 11. Образование молекулы НF
Более сложные d- и f-орбитали также характеризуются направлениями максимальной электронной плотности вдоль осей их симметрии.
Направленность связи хорошо иллюстрирует пример молекулы сероводорода Н 2 S:
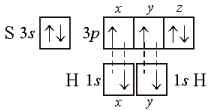
Поскольку оси симметрии валентных 3р-орбиталей атома серы взаимно перпендикулярны, то следует ожидать, что молекула Н 2 S должна иметь уголковую структуру с углом между связями S–Н 90° (рис. 12). Действительно, угол близок к расчетному и равен 92°.
 Рис. 12. Образование молекулы Н
2
S
Рис. 12. Образование молекулы Н
2
S
Направление ковалентных связей характеризуется валентными углами - углами между линиями, соединяющими связываемые атомы. Графическая формула химической частицы не несет информации о валентных углах. Например, в сульфат-ионе SO 4 2− валентные углы между связями сера−кислород равны 109,5 o , а в тетрахлоропалладат-ионе 2− − 90 o . Совокупность длин связей и валентных углов в химической частице определяет ее пространственное строение. Для определения валентных углов используют экспериментальные методы изучения структуры химических соединений. Оценить значения валентных углов можно теоретически, исходя из электронного строения химической частицы.
Таким образом, направленность – одно из основных свойств ковалентной связи.
Полярность и поляризуемость ковалентной связи.
Полярность химической связи зависит от разности электроотрицательностей связываемых атомов. Электроотрицательность − условная величина, характеризующая способность атома в молекуле притягивать электроны. Если в двухатомной молекуле А−В образующие связь электроны притягиваются к атому В сильнее, чем к атому А, то атом В считается более электроотрицательным. Шкала электроотрицательности была использована Л. Полингом для количественной характеристики способности атомов к поляризации ковалентных связей. Самое высокое значение электроотрицательности имеет фтор. Наименее электроотрицательный элемент - цезий. Чем выше значение разности электроотрицательностей двух атомов, тем более полярной является химическая связь между ними. В зависимости от того, как происходит перераспределение электронной плотности при образовании химической связи, различают несколько ее типов. Предельный случай поляризации химической связи - полный переход электрона от одного атома к другому. При этом образуются два иона, между которыми возникает ионная связь. Для того чтобы два атома смогли создать ионную связь, необходимо, чтобы их электроотрицательности очень сильно различались. Если электроотрицательности атомов равны (при образовании молекул из одинаковых атомов), связь называют неполярной ковалентной .
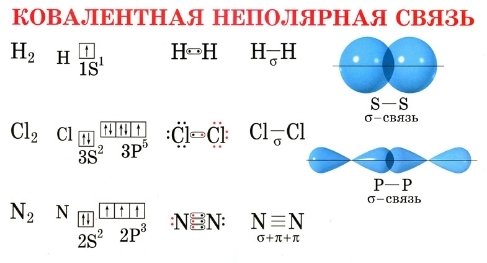
Рис.13. Ковалентная неполярная связь.

Рис.14. Ковалентная полярная связь.
Чаще всего встречается полярная ковалентная связь - она образуется между любыми атомами, имеющими разные значения электроотрицательности. Количественной оценкой полярности ("ионности") связи могут служить эффективные заряды атомов. Эффективный заряд атома характеризует разность между числом электронов, принадлежащих данному атому в химическом соединении, и числом электронов свободного атома. Атом более электроотрицательного элемента притягивает электроны сильнее. Поэтому электроны оказываются ближе к нему, и он получает некоторый отрицательный заряд, который называют и эффективным, а у его партнера появляется такой же положительный заряд.
Гибридизация ковалентной связи .
Гибридизация орбиталей - это изменение формы некоторых орбиталей при образовании ковалентной связи для достижения более эффективного перекрывания орбиталей.
sp 3 - Гибридизация . Одна s - орбиталь и три p - орбитали превращаются в четыре одинаковые "гибридные" орбитали, угол между осями которых равен 109 ° 28".
Рис.15. sp 3 - Гибридизация .sp 3 - гибридизация, имеют тетраэдрическую геометрию (CH 4 , NH 3 ).
sp 2 - Гибридизация. Одна s - орбиталь и две p - орбитали превращаются в три одинаковые "гибридные" орбитали, угол между осями которых равен 120 ° .
Рис. 16. sp 2 - Гибридизация .Если связь образуется при перекрывании орбиталей по линии, соединяющей ядра атомов, она называется s - связью. Если орбитали перекрываются вне линии, соединяющей ядра, то образуется p - связь. Три sp 2 - орбитали могут образовывать три s - связи ( BF 3 , AlCl 3 ). Еще одна связь (p - связь) может образоваться, если на p - орбитали, не участвующей в гибридизации, находится электрон (этилен C 2 H 4 ).
Молекулы, в которых осуществляется sp 2 - гибридизация, имеют плоскую геометрию.
sp - Гибридизация. Одна s - орбиталь и одна p - орбиталь превращаются в две одинаковые "гибридные" орбитали, угол между осями которых равен 180 ° .
Рис.17. sp - Гибридизация .Две sp - орбитали могут образовывать две s - связи (BeH 2 , ZnCl 2 ). Еще две p - связи могут образоваться, если на двух p - орбиталях, не участвующих в гибридизации, находятся электроны (ацетилен C 2 H 2 ).
Молекулы, в которых осуществляется sp - гибридизация, имеют линейную геометрию.
3.Донорно-акцепторный механизм образования ковалентной связи
Все рассмотренные нами выше молекулы веществ образованы по обменному механизму. Однако нельзя забывать о еще одном способе образования ковалентной связи – донорно-акцепторном.
Пара электронов с антипараллельными спинами, образующая связь, может быть получена не только по обменному механизму, предусматривающему участие электронов обоих атомов, но и по иному механизму, называемому донорно-акцепторным: один атом (донор) предоставляет для образования связи неподеленную пару электронов, а другой (акцептор) – вакантную квантовую ячейку:

Рис. 18. Механизмы образования ковалентной связи.
Результат по обоим механизмам получается одинаковый. Часто образование связи можно объяснить и тем, и другим механизмом. Например, молекулу НF можно получить не только в газовой фазе из атомов по обменному механизму, как показано выше (рис. 18 ), но и в водном растворе из ионов Н + и F – по донорно-акцепторному механизму:

Вне сомнений, молекулы, полученные по разным механизмам, неразличимы; связи совершенно равноценны. Поэтому правильнее не выделять донорно-акцепторное взаимодействие в особый вид связи, а считать его лишь особым механизмом образования ковалентной связи.
Когда хотят подчеркнуть механизм образования связи именно по донорно-акцепторному механизму, ее обозначают в структурных формулах стрелкой от донора к акцептору (D®А). В других случаях такую связь не выделяют и обозначают черточкой, как и по обменному механизму: D–А.
Связи в ионе аммония, образующегося по реакции: NH 3 + H + = NH 4 + ,
выражаются следующей схемой:

Структурную формулу NН 4 + можно представить как
 .
.
Вторая форма записи предпочтительней, поскольку отражает экспериментально установленную равноценность всех четырех связей.
Образование химической связи по донорно-акцепторному механизму расширяет валентные возможности атомов: валентность определяется не только числом неспаренных электронов, но и числом неподеленных электронных пар и вакантных квантовых ячеек, участвующих в образовании связей. Так, в приведенном примере валентность азота равна четырем.
Донорно-акцепторный механизм успешно используется для описания связи в комплексных соединениях по методу ВС.
Литература.
Ахметов Н. С. Неорганическая химия. - изд. 2-е перераб. и доп.. - М.: Высшая школа, 1975.
Габриелян. О.С., Остроумов И.Г. Химия. – М.: «Дрофа», 2008.
http://www.km.ru/referats/B496925228A344ECA85A5BA4B17AA5B2
Химическая связь между атомами, осуществляемая обобществленными электронами, называется ковалентной связью. Ковалентная связь является универсальным типом химической связи.
Ковалентная связь существует между атомами как в молекулах, так и в кристаллах. Она возникает как между одинаковыми атомами, так и между разными атомами. Характерными особенностями ковалентной связи являются её насыщаемость и направленность. Насыщаемость ковалентных связей обусловлена тем, что в химическом взаимодействии участвуют электроны только внешних энергетических уровней, т. е. ограниченное число электронов.
Электронные облака атомов имеют определенную пространственную ориентацию. Соответственно и область перекрывания электронных облаков находится в определенном направлении по отношению к взаимодействующим атомам. Поэтому ковалентная связь обладает направленностью. Характер распределения электронной плотности при образовании связи зависит от вида взаимодействующих атомов.
Особенности КС:
1. Прочность КС – это свойства характер. длинной связи (межъядерное пространство) и энергии энергией связи.
2. Полярность КС . Различают ковалентную полярную и неполярную связи. Полярная- образуется между атомами с разной ЭО. ОЭО>0. Неполярная – образуется между атомами с одинаковой ЭО. ОЭО=0
3. Насыщаемость КС – это способность атома участвовать только в определенном числе КС, насыщаемость характеризует валентностью атома. Количественные меры валентности явл. число не спаренных электронов у атома в основном и в возбужденном состоянии.
4. Направленность КС. Наиболее прочные КС образуются в направлении максимального перекрывания атомных орбиталей, т.е. мерой направленности служит валентный угол.
5. Гибридизация КС – при гибридизации происходит смещение атомных орбиталей, т.е. происходит выравнивание по энергии и по форме. Существует sp, sp 2 , sp 3 – гибридизация. sp – форма молекулы линейная (угол 180 0), sp 2 – форма молекулы плоская треугольная (угол 120 0), sp 3 - форма тетраэдрическая (угол 109 0 28).
6. Кратность КС или делоколизация связи – Число связей, образующихся между атомами, называется кратностью (порядком) связи. С увеличением кратности (порядка) связи изменяется длина связи и ее энергия.
Конец работы -
Эта тема принадлежит разделу:
При химическом взаимодействии атомов образуются молекулы. Молекулы
Химия наука о строении свойствах веществ их превращениях и сопровождающих явлениях Три главные задачи исследование строения вещества... Различают неорганическую органическую и элементоорганическую химии Объектом... Химия является общетеоретической дисциплиной Она призвана дать современное научное представление о веществе как одном...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ:
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Все темы данного раздела:
Модель атома.
1.Первая модель М.П. Морозова была разработана в 1860 г. – атом некий кристалл в узлах находятся электроны, в середине сосредоточен «+» заряд.
2.Э. Резерф
Вопрос 3. Квантово-механическое представление о строении атома. Квантовые числа и их физический смысл.
Волновая механика описывает движение ℮ в атоме как распространение волны по всему объему атома. Каждое мгновение ℮ может находиться в любой части пространства вокруг ядра. Область прост
Вопрос 4. Распределение электронов в многоэлектронном атоме. Принцип Паули. Правило Гунда. Порядок заполнения электронных подуровней.
Распределения электронов в многоэлектронных атомах основано на трех положениях: принципе минимума энергии, принципе В. Паули, и правиле В. Хунда
Принцип минимума энергии:э
Вопрос 7. Обменный и донорно-акцепторный механизм образования ковалентной связи.
Механизм возникновения ковалентных связей путем обобществления неспаренных электронов двух атомов получил название обменного механизма. Образование ковалентной связи может происход
Вопрос 9.Методы молекулярных орбиталей (ММО) и валентных связей(МВС). Сравнительная характеристика ММО и МВС.
ММО- химическая связь рассматривается как многоэлектронная и многоцентровая. В молекуле образуется собственная система молекулярных орбиталей, на которых находятся все электроны данной молекулы.
Вопрос 11. Водородная связь и межмолекулярное взаимодействие.
Водородная связь.возникает между положительно поляризованным атомом водорода и отрицательно поляризованным атомом с большой электроотрицательностью.
Положительно поляризо
Вопрос 13. Химичёская термодинамика, термодинамические параметры (Т, р, V). Внутренняя энергия. Первый закон термодинамики.
Химическая термодинамикаизучает переходы химической энергии в другие формы - тепловую, электрическую и т. п., устанавливает количественные законы этих переходов, а также направлен
Вопрос 14. Энтальпия образования вещества. Закон Гесса и его применение.
Стандартная энтальпия образования вещества- это тепловой эффект образования одного моля сложного вещества из простых веществ устойчивых при стандартных условиях и данной температуре.
Физический смысл энергии Гиббса
Изменение свободной энергии равно максимально полезной работе, которую совершает система в изобарно-изотермическом процессе.
По энергии Гиббса мы можем определить самопроизвольность протек
Вопрос 18. Влиятние температуры на скорость химической реакции. Правило Вант-Гоффа. Энергия активации. Уравнение Аррениуса.
Повышение температуры ускоряет большинство химических реакций. Согласно правилу Вант-Гоффа при повышении температуры на 10 К скорость многих реакций увеличивается в 2-4
Вопрос19. Гомогенный и гетерогенный катализ. Катализаторы и ингибиторы
Катализ-химическое явление,суть которого заключается в изменении скоростей хим.реакций при воздействии некоторых в-в. (бывает неорганический:автокатализ,гетерогенный и гомогенн
Вопрос 20.Химическое равновесие. Смещение хим.равновесия при изменении условий протекания хим.процессов. Принцип Ле-Шателье.
Химическое равновесие-неизменное во времени состояние сис-мы,содержащая в-ва способные к хим.взаимодействию =
Константа равновесия ()- это отношение произведен
Вопрос 21. Растворы. Свойства растворов
Растворы –это гомогенная система переменного состава, состоящая из двух или более компонентов. Растворы могут быть жидкими (морская вода), газообразными (воздух) и твердыми (сплавы
Вопрос 22. Способы выражения концентраций растворов
Концентрация-кол-во растворенного в-ва в определенном объеме раствора или растворителя.
Процентрая концентрация или массовая доля, -отношение массы врастворенного в-ва к мас
Законы растворов- это и есть законы Рауля!
Первый закон Рауля: Величина относительного понижения давления пара над раствором по сравнению с чистым растворителем пропорционально концентрации растворенного вещества ∆Р=(Р
Вопрос 24. Закон Рауля. Осмос. Физический смысл эбуллиоскопической и криоскопической постоянной.
Закон Рауля: Величина относительного понижения давления пара над раствором по сравнению с чистым растворителем пропорционально концентрации растворенного вещества ∆Р=(Р0-Р)/Р0
Вопрос 25. Растворы электролитов. Электролитическая диссоциация. Степень диссоциации. Константа диссоциации.
Электролиты – это вещества, которые проводят эл. ток если они находятся в растворенном или расплавленном состояниях. Носителями электричества в растворе являются анионы(-), катионы
Вопрос 27 Ионное произведение воды. Водородный показатель (рН) растворов.
H2O ↔ H+ + OH¯.
Кд = =1.8 · 10-16
=55,56 моль
Ионное произведение воды:
Водородным
Вопрос 29.Гидролиз солей. Константа гидролиза. Степень гидролиза.
Солями называются электролиты, при диссоциации кот образуются катионы металлов и анионы кислотных остатков.
Гидролизом солей называют реакции обмена межу водой и растворенным
Вопрос 30. Дисперсные системы. Коллоидные растворы, свойства.
Дисперсные системы –гетерогенная система, состоящая из 2 или более фаз с сильноразвитой поверхностью раздела между ними.
Вещество, которое в дисперсионной системе образует
Коллоидные растворы.
Частицы дисп.фазы кол.растворов наз-т кол-ми частицами. Коллоидные частицы несут на себе заряд, что обуславливает притяжение к ним диполей воды. На поверхности частицы созд-ся гидратная оболочка. С
Вопрос 31. Строение мицеллы коллоидов. Оптические и электрические свойства коллоидных растворов.
Мицеллы-частицы в коллоидных системах,состоящие из нерастворимого в данной среде ядра очень малого размера,окруженного очень малой оболочкой адсорбированных ионов и молекул растворите
Вопрос 33. Электродный потенциал. Старндартный электродный понетциал.Водородный потенциал.Уравнение Нернста.
Электрод-любой тонкопроводящий материал,погруженный в раствор электролита.
При установлении равенства между металлом и раствором возникает разность потенциалов, которая наз-с
Водородный потенциал???
Уравнение Ненста-уравненик,связывающее окислит-восстановит потенциал сис-мы с активностями в-в,входящих в электрохим.ур-е,и стандартным электродным потенциалом окислит-восстано.пар.OX+ne
Вопрос 34. Гальванический элемент: устройства, протекающие процессы на аноде и катоде. ЭДС и энергия Гиббса гальванического элемента
Гальванический элемент-совокупность последовательно соединенных проводников,из которых хотя бы один явл-ся проводником второго рода,т.е. электролитом.
Гальванический элеме
Вопрос 35. Электролиз. Законы Фарадея. Электрохимический эквивалент. Выход по току.
Электролиз – ОВ процесс, протекающий при прохождении тока через раствор или расплав электролита.
При электролизе происходит превращение эл. энергии в химическую.
Вопрос 37. Поляризация, ее причины. Перенапряжение.
Равновесные потенциалы электродов могут быть определены в условиях отсутствия в цепи тока. При прохождении электрического тока потенциалы электродов изменяются. Изменение потенциала электрода при
Химическая связь – важнейшее понятие химии, позволяющее описать более детально химические свойства соединений, а также их строение и физические свойства. Химическая связь - это взаимодействие атомов, обусловливающее устойчивость химической частицы или кристалла как целого. Химическая связь образуется за счет электростатического взаимодействия между заряженными частицами: катионами и анионами, ядрами и электронами. При сближении атомов начинают действовать силы притяжения между ядром одного атома и электронами другого, а также силы отталкивания между ядрами и между электронами. На некотором расстоянии эти силы уравновешивают друг друга, и образуется устойчивая химическая частица. Основные характеристики химической связи:
Энергией связи – называют ту энергию, которую необходимо затратить для ее разрыва. При этом молекула должна находиться в основном (невозбужденном) состоянии. Эта величина определяет прочность связи. Чем больше энергия, затрачиваемая на разрыв связи, тем прочнее связь. Единица измерения энергии связи - кДж/моль. Например, энергия связи Н-Н в молекуле водорода равна 436 кДж/моль. Если в молекуле несколько одинаковых связей, то, очевидно, для разрушения каждой следующей потребуется различная энергия и в таком случае говорят о средней энергии связи.
Длина связи – расстояние между ядрами атомов в соединении (нм)
Полярность связи - смещение электронного облака в сторону более электроотрицательного атома.
Валентные углы - Это углы между связями в молекуле. Их схематически можно представить как углы между прямыми линиями, соединяющими ядра атомов в молекуле. Эти воображаемые прямые, проведенные через два ядра, называют линиями связи. Величины валентных углов зависят от природы атомов и характера связи. Простые двухатомные молекулы всегда имеют линейную структуру. Трехатомные и более сложные молекулы могут обладать различными конфигурациями. Например, в молекуле воды угол между линиями связи Н-О равен 104,5°, а в сходной молекуле сероводорода валентный угол между связями составляет 92°. Совокупность длин связей и валентных углов в химической частице определяет ее пространственное строение.
Насыщаемость - свойство атома образовывать не любое, а определенное число связей с другими атомами.
Направленность – свойство, зависящее от направления перекрывания атомных орбиталей (АО). сигма - связи возникают при перекрывании АО вдоль линии связи, соединяющей ядра атомов; пи - связи образуются при перекрывании АО вне линии, соединяющих ядра атомов.
Кратность связи – число связей между атомами двух элементов. Чем больше кратность связи, тем больше энергия связи и тем меньше длина связи.
7. Ковалентная связь (КС). Условия образования ковалентной связи, механизмы образования, свойства связи, критерий прочности.
КС – связь, осуществляемая за счет электронной пары, принадлежащей обоим атомам.
Условия образования КС : она образуется между атомами с высокой электроотрицательностью. (электоротр-ть – способность атомов притягивать к себе электроны).
∆Χ – разность электроотрицательности 2-х атомов, если ∆Χ≤1.4, связь полярная
КС м.б. образована:
1 – между любыми атомами неметаллов (т.к. у всех неметаллов высокие значения электроотр-ти), пр: HCl, значения электроотр-ти – по таблицам, у Н=2.1, у Cl=3.1, - ∆Χ=3.1-2.1=1≤1.4, это связь ковалентная и полярная.
2 – между атомами неметалла и металла, если металл находится в высокой степени окисления, пр: CrCl6 для Cr=2.4, ∆Χ=3.1-2.4=0.7≤1.4 - это ковалентная полярная связь.
Механизмы образования КС :
1- обменный механизм - 2 атома обмениваются электронами, образуя общую электронную пару, принадлежащую обоим и называемую «поделенная». Примером могут служить молекулы летучих неорганических соединений: НСl, Н 2 О, Н 2 S, NН 3 и др. Образование молекулы НСl можно представить схемой Н. + . Сl: = Н:Cl: Электронная пара смещена к атому хлора, так как относительная электроотрицательность атома хлора (2,83) больше, чем атома водорода (2,1).
2 – донорно-акцепторный механизм : - заключается в том, что пара электронов одного атома (донора) занимает свободную орбиталь другого атома (акцептора) Рассмотрим в качестве примера механизм образования иона аммония . В молекуле аммиака атом азота имеет неподеленную пару электронов двухэлектронное облако): .
У иона водорода свободна (не заполнена) 1s-орбиталь, что можно обозначить как □H+. При образовании иона аммония двухэлектронное облако азота становится общим для атомов азота и водорода, т.е. оно превращается в молекулярное электронное облако. А значит, возникает четвертая ковалентная связь. Процесс образования иона аммония можно представить схемой
| + □H+ → |
Заряд иона водорода становится общим (он делокализован, т.е. рассредоточен между всеми атомами), а двухэлектронное облако (неподеленная электронная пара), принадлежащее азоту, становится общим с водородом.
Ковалентная связь бывает полярной (сложные молекулы) и неполярной (простые молекулы).
Свойства ковалентной связи
Ковалентная связь обладает рядом важных свойств. К их числу относятся: насыщаемость и направленность.
Насыщаемость - характерное свойство ковалентной связи. Она проявляется в способности атомов образовывать ограниченное число ковалентных связей. Это связано с тем, что одна орбиталь атома может принимать участие в образовании только одной ковалентной химической связи. Данное свойство определяет состав молекулярных химических соединений. Так, при взаимодействии атомов водорода образуется молекула Н 2 , а не Н 3 . Третий атом водорода не может присоединиться, так как спин его электрона окажется параллельным спину одного из спаренных электронов в молекуле. Способность к образованию того или иного числа ковалентных связей у атомов различных элементов ограничивается получением максимального числа неспаренных валентных электронов.
Направленность - свойство ковалентной связи, определяющее геометрическую структуру молекулы. Причина направленности связи заключается в том, что перекрывание электронных орбиталей возможно только при их определенной взаимной ориентации, обеспечивающей наибольшую электронную плотность в области их перекрывания. В этом случае образуется наиболее прочная химическая связь.
8. Перекрывание атомных орбиталей как условие образования связи. Типы перекрывания (сигма, пи). Гибридизация атомных орбиталей. Кратные связи.
Химическая связь между атомами обусловливается перекрыванием электронных облаков.
Перекрывание атомных орбиталей вдоль линии, связывающей ядра атомов, приводит к образованию σ-связей. Между двумя атомами в химической частице возможна только одна σ-связь. Все σ-связи обладают осевой симметрией относительно межъядерной оси. Совокупность направленных, строго ориентированных в пространстве σ-связей создает структуру химической частицы.
При дополнительном перекрывании атомных орбиталей, перпендикулярных линии связи, образуются π-связи.
Связь двух атомов может осуществляться более чем одной парой электронов. В результате этого между атомами возникают кратные связи:
| Одинарная (σ) | Двойная (σ +π) | Тройная (σ + π + π) |
| F−F | O=O | N≡N |
Гибридизация атомных орбиталей
При определении геометрической формы химической частицы следует учитывать, что пары внешних электронов центрального атома, в том числе и не образующие химическую связь, располагаются в пространстве как можно дальше друг от друга.
Сущность гибридизации атомных орбиталей состоит в том, что электрон вблизи ядра связанного атома характеризуется не отдельной атомной орбиталью, а комбинацией атомных орбиталей с одинаковым главным квантовым числом. Такая комбинация называется гибридной (гибридизованной) орбиталью. Как правило, гибридизация затрагивает лишь высшие и близкие по энергии атомные орбитали, занятые электронами.
В результате гибридизации появляются новые гибридные орбитали (рис.24), которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары (или неспаренные электроны) оказались максимально удаленными друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. Поэтому тип гибридизации определяет геометрию молекулы или иона.
ТИПЫ ГИБРИДИЗАЦИИ
Ковалентная связь характеризуется направленностью в пространстве, полярностью, кратностью, энергией и длиной.
Как мы знаем, электронные орбитали (кроме s-орбиталей) имеют пространственную направленность . Ковалентная связь, которая является результатом электронно-ядерных взаимодействий, располагается в определенном направлении по отношению к ядрам этих атомов. Если электронные облака перекрываются в направлении прямой, которая соединяет ядра атомов (т. е. по оси связи), такая ковалентная связь называется s-связью (сигма-связью). Например, в молекулах Н 2 , Cl 2 , HC1 атомы соединяются ковалентной s-связью. Ковалентные сигма-связи образуются при перекрывании орбиталей: s - s (как в Н 2): s - р (как в НС1), р - р (как в С1 2).
При перекрывании p-орбиталей, направленных перпендикулярно оси связи, образуются две области перекрывания по обе стороны оси связи. Такая ковалентная связь называется p-связью (пи-связью) (рис. 6). Например, в молекуле азота атомы связаны одной s-связью и двумя p-связями (рис. 7).
Рис. 6. Схематическое изображение p-связи
Рис. 7. Схематическое изображение s- и p-связей в молекуле азота
Направленность ковалентной связи определяет пространственную структуру молекул, т. е. их форму. Молекула хлороводорода имеет линейную форму: она образована с помощью одной s-связи (s - р-орбитали). Молекула воды имеет угловое строение: она образуется за счет перекрытия s-орбиталей двух атомов водорода с двумя взаимно перпендикулярными р-орбиталями атома кислорода (рис. 8). Следовательно, угол между s-связями в молекуле воды должен быть равен 90°. В действительности угол равен 104,5°, что объясняется явлением гибридизации. Молекула аммиака имеет форму правильной пирамиды, молекула метана - форму тетраэдра.
Рис. 8. Строение молекулы воды
Полярность связи определяется асимметрией в распределении общего электронного облака вдоль оси связи.
Если общие электронные пары располагаются симметрично относительно обоих ядер, то такая ковалентная связь называется неполярной.
В молекулах простых веществ - водорода Н 2 , кислорода О 2 , азота N 2 , хлора С1 2 , фтора F 2 атомы соединяются неполярной ковалентной связью.
Если общие электронные пары смещаются к одному из атомов (располагаются несимметрично относительно ядер различных атомов), то такая ковалентная связь называется полярной.
Связь в молекулах воды Н 2 О, аммиака NH 3 , хлороводорода НС1- полярная.
Кратность ковалентной связи определяется числом общих электронных пар, которые связывают атомы.
Связь между двумя атомами при помощи одной пары электронов называется простой (связи Н - С1,С - Н,Н - О и т. д.). Связь между двумя атомами при помощи двух электронных пар называется двойной. Связь между двумя атомами при помощи трех электронных пар называется тройной.
Например, двойная связь наблюдается между атомами углерода в этилене Н 2 С = СН 2 , тройная связь наблюдается в молекулах азота N N, ацетилена Н - С С - Н.
Длина связи - это равновесное расстояние между ядрами атомов. Длину связи выражают в нанометрах (нм). Чем меньше длина связи, тем прочнее химическая связь. Мерой прочности связи является ее энергия.
Энергия связи равна работе, которую необходимо затратить на разрыв связи. Выражают энергию связи в килоджоулях на моль (кДж/моль); например, в молекуле водорода энергия связи равна 435 кДж/моль. Энергия связи увеличивается с уменьшением длины связи (табл. 10).
Таблица 10. Вид, длина и энергия связи в молекулах некоторых веществ
Энергия связи увеличивается с увеличением кратности связи (табл. 11).
Таблица 11. Длина и энергия связи между атомами азота и между атомами углерода
Процесс образования связи протекает с выделением энергии (экзотермический процесс), а процесс разрыва связи - с поглощением энергии (эндотермический процесс).
Полярность молекул
Полярность молекул зависит от полярности отдельных связей и от их расположения в молекуле (т. е. от строения молекул).
Молекулы простых веществ (Н 2 , F 2 , N 2 и др.), образованные неполярными ковалентными связями, неполярны .
Молекулы сложных веществ могут быть и неполярными и полярными. Примеры веществ с неполярными молекулами: диоксид углерода СО 2 , метан СН 4 , бензол С 6 Н 6 , глюкоза С 6 Н 12 О 6 , диметиловый эфир С 2 Н 6 О и др. Примеры веществ с полярными молекулами: диоксид серы SO 2 , вода Н 2 О, аммиак NH 3 , этиловый спирт С 2 Н 5 ОН и др.
В неполярных молекулах «центр тяжести» электронного облака совпадает с «центром тяжести» положительного заряда ядер. В полярных молекулах «центр тяжести» электронного облака не совпадает с «центром тяжести» положительного заряда.
Например, в молекуле хлороводорода НС1 электронная плотность около ядра хлора выше, чем около ядра водорода, т. е. атом хлора имеет отрицательный заряд q = - 0,18, а атом водорода положительный заряд q -= + 0,18. Заряды (q) атомов в молекуле называют .эффективными. Поэтому полярные молекулы можно рассматривать как электрические диполи, в которых заряды, разные по знаку, но одинаковые по величине, расположены на определенном расстоянии друг от друга. Мерой полярности молекул является электрический момент диполя.
Электрический момент диполя - это произведение эффективного заряда на расстояние между центрами положительного и отрицательного зарядов в молекуле. Электрический момент диполя в молекуле зависит от ее структуры. Наличие или отсутствие электрического момента диполя позволяет судить о геометрическом строении молекулы. Например, молекула СО 2 неполярна, а молекула SO 2 обладает электрическим моментом диполя. Отсюда следует, что молекула СО 2 имеет линейное строение, а молекула SO 2 - угловое.
Свойства веществ зависят от полярности молекул. Вещества, молекулы которых полярны, имеют температуры кипения и плавления выше, чем вещества, молекулы которых неполярны. Это объясняется взаимным притяжением полярных молекул.
Электроотрицательность
Способность атомов химического элемента притягивать к себе общие электронные пары называется электроотрицательностью.
Электроотрицательность элемента определяется суммой его энергии ионизации и сродства к электрону. Относительные электроотрицательности атомов некоторых элементов приведены в табл. 12.
Таблица 12. Относительные электроотрицательности некоторых элементов
| Период | Группа | ||||||
| I | II | III | IV | V | VI | VII | |
| Н 2,1 | |||||||
| Li 0,98 | Be 1.5 | В 2,0 | С 2,5 | N 3,07 | О 3.50 | F 4,0 | |
| Na 0,93 | Mg 1,2 | Al 1,6 | Si 1,9 | P 2,2 | S 2,6 | Cl 3,0 | |
| К 0.91 | Са 1,04 | Ga 1,8 | Ge 2,0 | As 2,1 | Se 2.5 | Br 2,8 | |
| Rb 0,89 | Sr 0,99 | In 1.5 | Sn 1.7 | Sb 1.8 | Те 2,1 | I 2,6 |
Чем больше электроотрицательность атома, тем сильнее притягивает он общую электронную пару. Когда между двумя атомами разных элементов образуется ковалентная связь, общие электронные пары смещаются к более электроотрицательному атому. Например, в молекуле воды Н 2 О общие электронные пары смещаются к атому кислорода.
Относительная электроотрицательность атома не является строго постоянной величиной и применяется только для определения направления смещения общих электронных пар при образовании молекул
Электроотрицательность элементов подчиняется периодическому закону. В периоде электроотрицательность элементов возрастает с увеличением порядкового номера элемента. В начале периода находятся элементы с низкой электроотрицательностью (металлы), а в конце периода элементы с наивысшей электроотрицательностью (неметаллы) В подгруппе электроотрицательность элементов уменьшается с увеличением порядкового номера. Самым электроотрицательным элементом в периодической системе является фтор У инертных элементов электроотрицательность отсутствует.
Химические элементы можно расположить в ряд в порядке возрастания электроотрицательности.
Sb, Si. В, As. H, Те. Р. С, Se, I, S, Br. Cl, N. О, F
электроотрицательностъ возрастает
Электроотрицательность характеризует различие свойств элементов. Поэтому ее используют как качественную характеристику при определении природы химической связи в различных соединениях.
Ионная связь
При образовании соединений из элементов, очень отличающихся по электроотрицательности (типичных металлов и типичных неметаллов), общие электронные пары полностью смещаются к более электроотрицательному атому. В результате образуются ионы.
Например, при горении натрия в хлоре неспаренный 3s-электрон атома натрия спаривается с 3p-электроном атома хлора. Общая электронная пара полностью смещается к атому хлора. В результате образуется натрий-ион Na + и хлорид-ион CI - .
Заряженные частицы, в которые превращаются атомы в результате отдачи или присоединения электронов, называют ионами.
Заряд отрицательного иона равен числу электронов, которые атом присоединил. Заряд положительного иона равен числу электронов, которые атом отдал.
Противоположно заряженные ноны притягиваются друг к другу.
Соединения, которые образуются из ионов, называются ионными. Связь между ионами называется ионной.
Между ионной и ковалентной связью нет резкой границы. Ионную связь можно рассматривать как крайний случай ковалентной полярной связи (рис. 9). В отличие от ковалентной ионная связь ненаправленна
Процесс отдачи электронов называется окислением. Процесс присоединения электронов называется восстановлением.
Например, при взаимодействии натрия с хлором атом натрия отдает электрон, окисляется и образуется натрий-ион Na – e - ®Na +
Рис 9. Схема перехода от ковалентной связи кионной
Атом хлора присоединяет электрон, восстанавливается и образуется хлорид-ион Cl + е - ®Сl - .
Металлы главных подгрупп I и II групп при соединении с неметаллами главной подгруппы VII группы образуют типичные ионные соединения. Например, хлорид натрия NaCl, фторид калия KF, хлорид кальция СаС1 2 .
Ионные соединения - твердые кристаллические вещества.
Водородная связь
Атом водорода, связанный с сильно электроотрицательным элементом (фтором, кислородом, азотом), может образовать еще одну связь с другим атомом сильно электроотрицательного элемента. Например, в молекуле воды атомы водорода связаны с атомами кислорода полярной ковалентной связью. Общие электронные пары смещаются к атому кислорода. Атом водорода имеет частичный положительный заряд, а атом кислорода частичный отрицательный. Положительно заряженный атом водорода одной молекулы воды притягивается отрицательно заряженным атомом кислорода другой молекулы воды. Между двумя атомами кислорода возникает связь, образованная с помощью атома водорода. Атом водорода находится на прямой, которая соединяет ядра этих атомов
O ¾ H. . . O ¾ H. . . O ¾ H. . . O ¾ H
Водородная связь образуется за счет сил электростатического притяжения полярных молекул друг к другу, особенно когда они содержат атомы сильно электроотрицательных элементов (F, O, N).
Например, водородные связи образуют HF, H 2 O, NH 3 , но не образуют их аналоги HCl, H 2 S, PH 3.
Водородные связи малоустойчивы и разрываются довольно легко (например, при плавлении льда и кипении воды), но так как на разрыв этих связей требуется затратить некоторую энергию, то температуры плавления и кипения веществ с водородными связями между молекулами оказываются значительно выше, чем у подобных веществ, но без водородных связей. Например:
(в HF и H 2 O есть водородные связи, а в HCl и H 2 S их нет).
Многие органические соединения также образуют водородные связи, важную роль водородная связь играет в биологических процессах.
У металлов самая низкая энергия ионизации. Поэтому в металлах валентные электроны легко отрываются от отдельных атомов и становятся общими для всего кристалла (обобществленными). Так образуются положительные ионы металла и электронный газ - совокупность подвижных электронов. В кристалле металла небольшое число обобществленных электронов связывает большое число ионов.
Химическая связь в металлах между положительными ионами и обобществленными электронами называется металлической связью.
Металлическая связь сходна с ковалентной. В основе образования этих связей лежат процессы обобществления валентных электронов. Но в металле валентные электроны являются общими для всего кристалла, а в соединениях с ковалентной связью общими являются только валентные электроны двух соседних атомов. Металлическая связь ненаправленна, так как валентные электроны распределены по кристаллу почти равномерно.
Металлическая связь характерна только для металлов в твердом или жидком агрегатном состоянии.